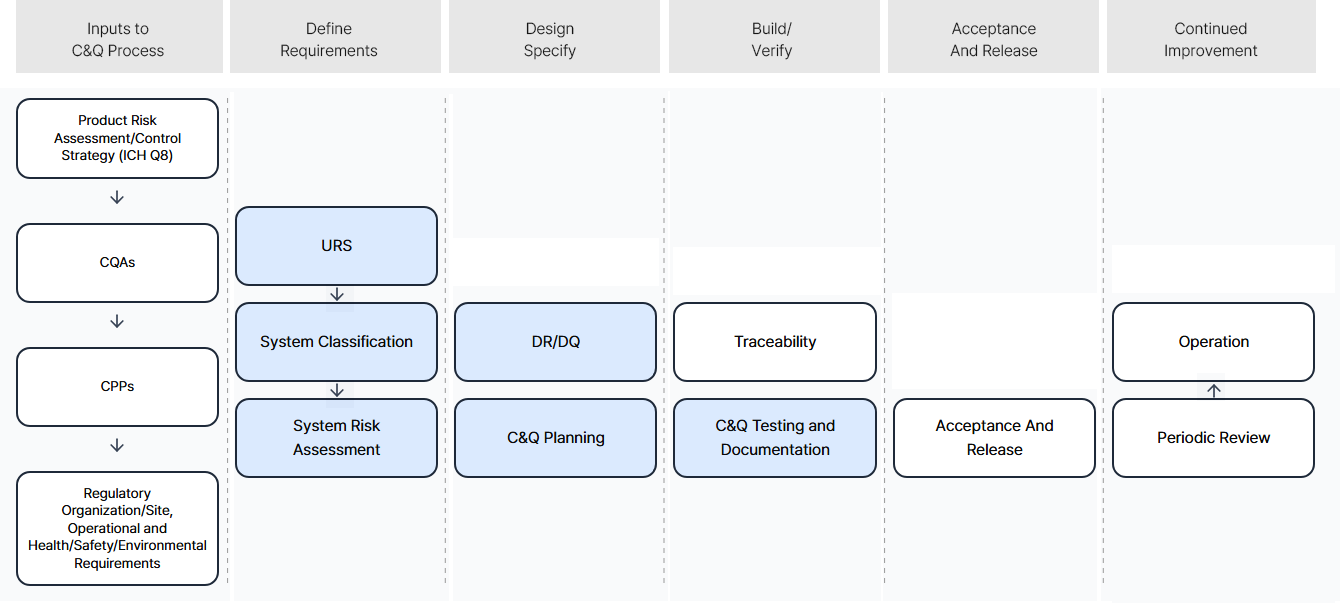
Science and Risk-Based C&Q Process
Science and Risk-Based C&Q Process는 의약품 제조 설비 및 시스템의 검증(밸리데이션)을 수행하는 현대적이고 효율적인 접근 방식입니다.
VIA는 기존의 모든 항목을 일률적으로 검사하는 방식에서 벗어나, 과학적 지식과 데이터를 바탕으로 제품의 품질과 환자의 안전에 직접적인 영향을 미치는 주요 리스크를 식별하고, 이에 자원을 집중하는 전략으로 비용 및 시간 절감과 효율성을 향상시키고 있습니다.
GAMP 5 기반의 IT 시스템(ERP, LIMS, MES) 검증
VIA는 GAMP 5(2nd Edition) 가이드라인에 따라 IT 시스템의 설계부터 운영, 폐기까지 전 수명 주기 (Lifecycle)를 검증하며, 고도화된 데이터 무결성 (Data Integrity) 솔루션을 제공합니다.
핵심 규제 대응 기술 Compliance Strategy) "21 CFR Part 11 EU GMP Annex 11 완벽 대응"
+ Audit Trail
+ User Access Control
+ Data Backup & Recovery
+ ALCOA+ Principle
규제 준수 및 데이터 무결성
(21 CFR Part 11, Annex 11)
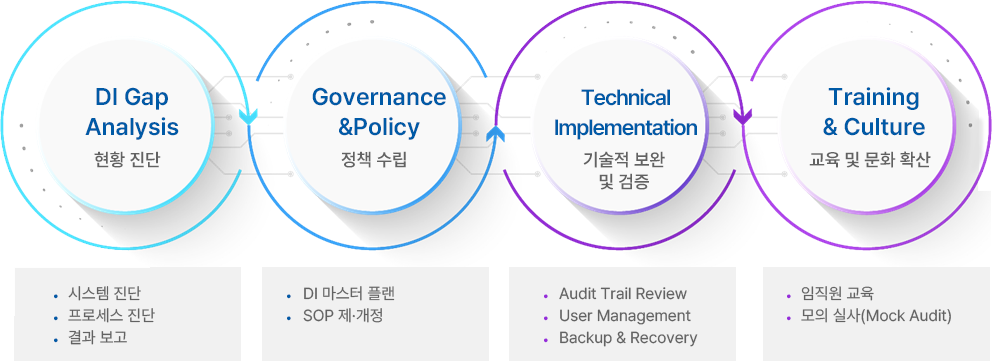
데이터 무결성 컨설팅 (Data Integrity)
최근 제약·바이오 산업에서 규제 기관(FDA, EMA, MFDS 등)이 가장 엄격하게 점검하는 항목은 데이터 무결성입니다.
모든 데이터 무결성 컨설팅은 국제 표준인 ALCOA+ 가이드라인을 기반으로 수행되며, 고객사의 규제 리스크를 실질적으로 해결할 수 있는 구체적인 컨설팅 모듈을 제안합니다.